
ISO13485是适用于医疗器械法规环境下的质量管理体系标准,其全称是《医疗器械 质量管理体系 用于法规的要求》。1996年ISO13485首次发布,2003年ISO/TC210发布了ISO13485:2003,应用于医疗器械领域。2015年ISO/TC210再次修订ISO13485,2016年3月ISO13485:2016正式发布。 ...

医疗器械CE认证新法规MDR中引入了一些新的概念,比如Basic UDI。Basic UDI是企业基于一定的编码规则(比如基于GS1),自己规定的一类产品的代码。这个代码不会出现在产品上 ...


医疗器械是有种类分的,不同的医疗器械产品对于CE认证的要求也是不同的。所以这篇文章会带来关于欧盟一类医疗器械CE认证流程,方便医药企业前来查阅。 ...
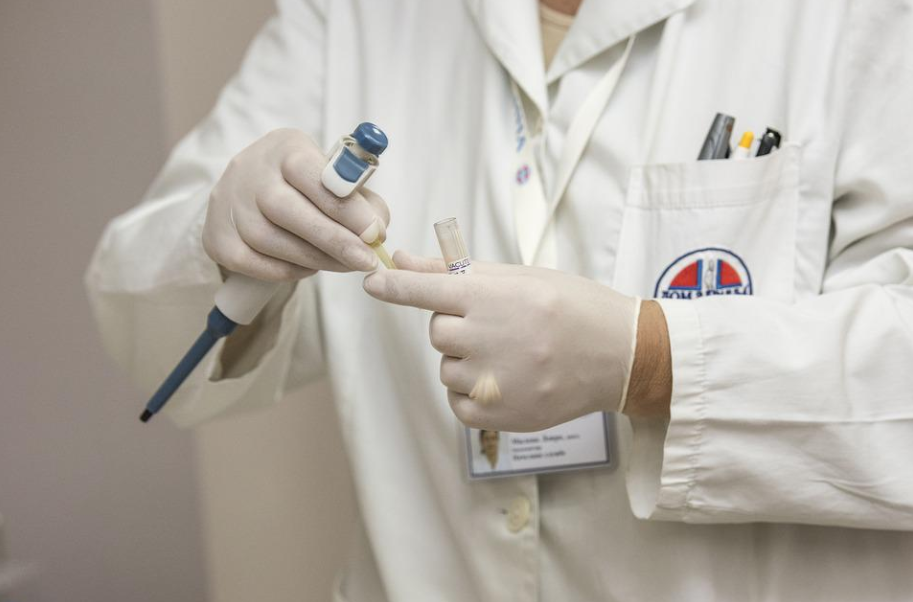
众所周知,欧盟市场在全球中属于主流的医疗器械市场之一,所以大部分的企业都会选择前往欧洲进行医疗注册服务。所以欧盟医疗器械CE认证服务包括哪些内容,也是很多人都想要了解的。本篇就带来详细的介绍,以便大家查阅。 ...

医用手套在申请医疗器械CE认证时,欧盟将医疗手套分成了I类非灭菌检查手套、I类灭菌检查手套、IIa类灭菌外科手套三类,三类产品的CE认证流程和要求见下图: ...
在新冠爆发以来,对于防疫物资的认证要求,CE认证也是有严格的相关要求。在此将内容展示,方便有想在欧洲市场的客户使用。 ...

在CE认证中,IVDR技术文档也是十分重要的。对于新型药企,可能不是特别了解其中的具体详情,所以在此将内容展示与此,方便大家需要。 ...

在很多企业进行医疗器械CE认证的时候,出口商会被要求提供欧盟自由销售证书,那么欧盟自由销售证书是什么?又要怎么办理?流程是什么样子的?也是很多人想要了解的,所以本篇文章就会大概的介绍一下具体情况。 ...
欧洲药品质量管理局(EDQM)对于已经收载到《欧洲药典European Pharmacopoeia》(简称EP)的原料药/辅料设置了一个独立的评价程序,称为“欧洲药典适用性认证”,即Certification of Suitability to Monograph of European Pharmacopoeia(早期简称COS,现称CEP)。通过欧洲药品质量管理局认证的原料 ...


